版權所有:北京歐仕科技有限公司(轉載需授權 )
藍藻藻華快速監(jiān)測技術解析
版權所有:北京歐仕科技有限公司(轉載需授權 )
工程師:王珊珊
藍藻藻華及其危害
隨著人類活動強度的加劇,大量的氮、磷等營養(yǎng)物質通過各種途徑進入河流、湖泊、海洋等水體,造成水體富營養(yǎng)狀態(tài)。有研究表明:我國目前66%以上的湖泊、水庫處于富營養(yǎng)化水平,其中22%處于重富營養(yǎng)和超富營養(yǎng)狀態(tài)(陳小峰等, 2014; 胡利靜等, 2015)。與富營養(yǎng)化伴生的一個生態(tài)災害現(xiàn)象是浮游植物藻華的大面積爆發(fā)(Farrow et al., 2020)。不同浮游植物類群形成的藻華會導致水體呈現(xiàn)出藍色、紅色、綠色、乳白色等不同的顏色,甚至有些物種會聚集形成絲狀體或片狀體,大面積的漂浮在水體表面,引發(fā)水體缺氧等一系列環(huán)境問題,嚴重時可能會導致魚類和其他水生生物的大量死亡(孔繁翔和高光, 2005; 王志剛, 2008; 莫婉湫等, 2009)。因此,水體富營養(yǎng)化現(xiàn)象以及由此形成的藻華災害已經成為我國湖泊目前與今后相當長一段時期內的重大環(huán)境問題。
在各種藻華中,藍藻藻華發(fā)生的范圍*廣、危害*大,對人體健康會造成較大的傷害,在世界各地及我國均有大量的報道(肖興富等, 2005; 胡傳林等, 2010; 李晟銘等, 2019)。藍藻門(Cyanophyta)與其他真核藻類門中的物種有明顯的區(qū)別:藍藻細胞沒有完整的細胞核結構,沒有核膜、核仁,僅有核質聚集在細胞的中央區(qū),被稱為原核細胞;沒有色素體等細胞器,通過分散在“核區(qū)”以外原生質內的色素進行光合作用,藻體結構簡單,單細胞藻體,各式群體和絲狀體;生活史中沒有有性生殖和具有鞭毛的生殖細胞(錢樹本等, 2005)。藍藻分布十分廣泛,遍布世界各地,但大多數(shù)物種是淡水的,海生的物種較少。
在世界范圍內,藍藻藻華發(fā)生的頻率與規(guī)模都呈現(xiàn)出迅猛的增長趨勢(陳雋, 2006)。在我國,不僅有許多富營養(yǎng)型的湖泊如太湖、巢湖、滇池等連年發(fā)生藍藻藻華,甚至在一些流速較大的河流中如錢塘江、漢江等也有藍藻藻華事件的發(fā)生(陸開宏, 2009)。發(fā)生在無錫的水污染事件就是因為水源地附近藍藻大量堆積,厭氧分解過程中產生了大量的氨氣、硫醇、硫醚以及硫化氫等異味化學物質導致(路云霞等, 2008; 楊銘威等, 2009)。如圖1 所示:N、P元素增多使得藍藻藻華爆發(fā),藍藻的大量繁殖消耗了水體中大量的溶解氧,進而使得生活在水體中的其他水生生物(魚類等)大量死亡,水質惡化,而魚類等死亡水生生物的骨架腐爛、分解又釋放出來大量的N、P營養(yǎng)鹽,形成了一個惡性循環(huán)。在許多情況下,藍藻可以在短時間內以極快的速度生長,故藻華發(fā)生的速度非常快,給環(huán)境監(jiān)測與預警預報帶來了很大的困難。
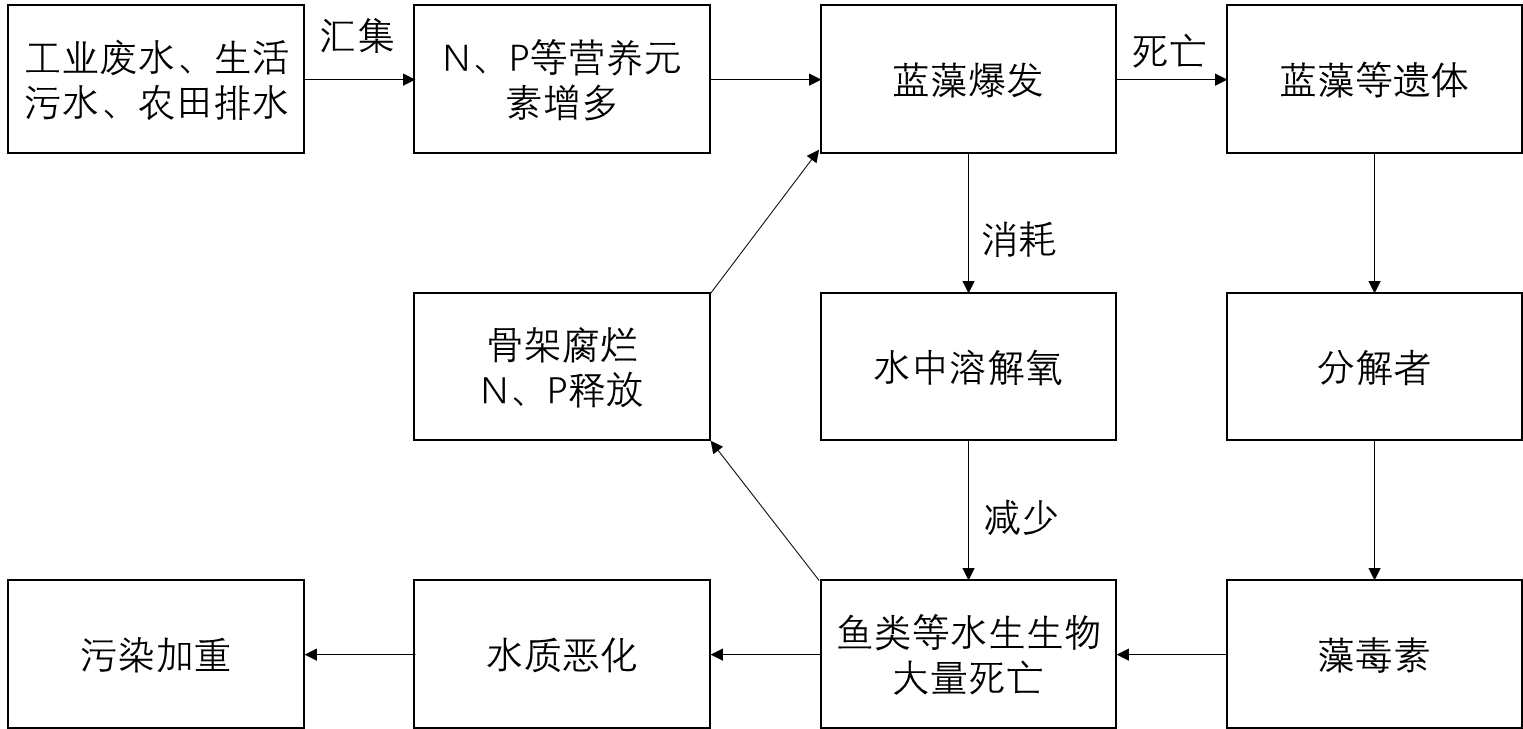
圖1 藍藻藻華爆發(fā)機理圖
鑒定藍藻的技術手段
藍藻藻華具有重大危害,但目前還缺少有效的治理手段。雖然有很多物理、化學和生物技術可以直接沉降或殺死形成藻華的藍藻細胞,或直接撈取大量聚集的藍藻,避免藍藻對水質的影響,但其所花費的人力物力十分巨大,且很難完全控制藍藻藻華對水質產生的影響。因此,必須建立一個藍藻藻華監(jiān)測系統(tǒng),以便環(huán)境管理部門提前采取技術措施,減少其帶來的影響。以供水為例,如果能提前數(shù)小時預測到藍藻藻華將在取水口聚集降解,就有足夠時間,及時采取包括水源水的調度和制水工藝的改進與強化等措施,減少藍藻藻華帶來的生態(tài)危害和健康風險,避免發(fā)生供水危機,保障供水安全(王志剛, 2008; 孔繁翔等, 2009)。
建立一個有效的藍藻藻華爆發(fā)預警系統(tǒng)需要解決以下幾個問題:
1) 監(jiān)測水體中是否存在藍藻?
2) 藍藻細胞的數(shù)量是多少?
3) 這些藍藻是否為有毒物種?
4) 藍藻毒素的濃度是多少?
5) 如何提前知道是否有問題?
藍藻群落的監(jiān)測內容主要是種類(是否含有有毒物種)與生物量(物種濃度是否超標)。傳統(tǒng)的監(jiān)測方法主要為人工鑒定,利用光學顯微鏡直接觀測藻類以獲得所需數(shù)據(jù)。通過形態(tài)學進行藻類鑒定至今仍是一種重要的技術手段,對于體積較大、具有特征形態(tài),便于區(qū)分的藻類,顯微鏡鏡檢已成為**方法。但是,顯微鏡觀察需要復雜的人工操作和專業(yè)的生物學分類知識,費時費力,易因觀察者的主觀判斷造成誤差,不能及時準確地反映水體污染狀況,且不能進行原位實時監(jiān)測,難以滿足種群動力學觀測量大、連續(xù)的要求,在實際應用中具有一定的局限性。另外,一些物種具有相似的形態(tài)學特征,在光學顯微鏡下很難分辨出來,可能需要借助電子顯微鏡,但檢測速度更慢,更難適用于大量樣品。
隨著光學儀器的發(fā)展,高效液相色譜儀、流式細胞儀已成為藻類多樣性分析的主要技術手段。通過分析藻類的細胞色素特征,可以得到定性及定量的結果,效率遠高于形態(tài)學鏡檢。隨著分子水平研究的迅猛發(fā)展,使得DNA分子鑒定方法逐漸成為一種新的藻類多樣性研究方法,其準確性方面都有著較大的優(yōu)勢。分子鑒定方法,首先需要選取被鑒定物種所含有的標記基因,通過DNA 測序進行序列的相似度比對,進而分析被檢測類群的多樣性。以上這些方法雖然誕生時間不同、發(fā)展速度差異較大,但具有不同的優(yōu)缺點,需要根據(jù)目標藻類的特征進行合理的選擇。表1列舉了常見藻類鑒定分析的技術及其特點(Trask et al., 2005; Lomas et al., 2011; 錢奎梅等, 2015; 孟溪, 2019)。
表1 藻類鑒定分析常用方法
技術方法 應用方面 測量速度 優(yōu)點 缺點
鏡檢 樣品少、直接計數(shù) 慢 準確度高且能較為全面地反映樣品的種類分布 耗時耗力;需有經驗的專業(yè)人員;水樣中的非藻顆粒會造成干擾
高效液相色譜 樣品多 慢 準確、便捷;可以確定藻類群落的組成和豐度 需前處理;受胞內物組成限制;藻類特征色素基礎性數(shù)據(jù)還比較缺乏
流式細胞儀 樣品多,直接計數(shù) 快 操作時間短,能靈敏檢測細胞死、活狀態(tài) 儀器昂貴;適用于小型細胞;鑒定水平低
分子鑒定 少量樣品 慢 準確度高 過程繁瑣,需要測序及PCR過程
FlowCam的優(yōu)勢
流式影像儀(Flow Cytometer and Microscope , FlowCam)將流式細胞技術、顯微成像技術和圖像采集技術相結合,具有連續(xù)成像和流式細胞計數(shù)的功能。因此,相比其他的技術手段,F(xiàn)lowCam具有自己獨特的優(yōu)勢,主要包括:
1) 快速計數(shù);
2) 高速顯示數(shù)字化的生物體圖像;
3) 多參數(shù)分析;
4) 建立圖像庫,實現(xiàn)自動分類;
5) 較好的區(qū)分生命體和非生命體;
6) 現(xiàn)場檢測。
FlowCam的應用案例
(1)綜合監(jiān)測
美國的一家飲用水機構為保證其用水安全,提出了一個綜合監(jiān)測藍藻細胞的方法,如圖2所示。首先,我們需要對水體中的藍藻細胞進行鑒定和計數(shù)。減少樣品測量時間的同時還要保證測量的準確性,**測量浮游生物的體型和豐度是評估和表征許多重要指標的必要手段。一些學者對FlowCam的準確性進行了對比試驗,如侯建軍等(2004)對實驗室培養(yǎng)的3種純種赤潮藻進行了不同計數(shù)方法(庫爾特計數(shù)法、FlowCam計數(shù)法、可見分光度法計數(shù)法、顯微鏡計數(shù)法)的比較研究,發(fā)現(xiàn)FlowCam在純種細胞計數(shù)方面有明顯的優(yōu)勢,是比較簡便、快捷、可行的細胞計數(shù)方法,且能人為分辨出細胞生長后期的細胞碎片甚至是死細胞。而準確計數(shù)微囊藻和魚腥藻等群體型和絲狀型藍藻細胞對監(jiān)測潛在的有毒藍藻至關重要。Lehman等(2017)準確計算了含有群體型微囊藻和絲狀型魚腥藻樣品的細胞密度。
當FlowCam檢測到樣品中微囊藻、魚腥藻和顫藻(這三種藍藻均產生毒素)濃度較高時,需對樣品進行qPCR檢測,以確認樣本中的藍藻菌是否有產生毒素的基因。樣本中有微囊藻細胞并不意味著就會有毒素的產生。如果產生毒素的基因不存在,或者沒有被激活,那么微囊藻毒素就不會存在。如果qPCR結果是陽性,存在產毒基因,之后要利用LC-MS/MS(液相色譜-質譜聯(lián)用儀)對樣品進行毒素檢測,分析樣品中毒素的濃度是否達到監(jiān)測標準。LC-MS/MS分析樣品成本較高,因此FlowCam數(shù)據(jù)和qPCR檢測結果聯(lián)合使用,以證明或放棄毒素檢測。
同時利用GC-MS(氣相色譜質譜聯(lián)用儀)來監(jiān)測飲用水中引起人類感官不悅的兩種典型嗅味物質:MIB(二甲基異茨醇)和GSM(土臭素)。一般認為GSM隨著魚腥藻數(shù)目的增加而增加。因此,當FlowCam計數(shù)魚腥藻細胞超過200個/ mL時,則表明嗅味事件可能已迫在眉睫。當GC-MS結果確認存在嗅味物質時,便開始用PAC(粉末活性炭)處理,以去除MIB和GSM。

圖2 監(jiān)測有毒藍藻的流程圖
(2)治理檢測
現(xiàn)有的除藻方法有化學除藻法、生物除藻法和物理除藻法。化學除藻法是利用化學試劑對藻類進行殺除,但化學試劑處理過程中,可能會使藍藻細胞的降解,進而導致有毒物質(微囊藻毒素等)、惡臭代謝物(MIB、GSM)等釋放到水體中,造成環(huán)境的二次污染,使水質環(huán)境形成惡性循環(huán)(孔繁翔等, 2009)。Jason等(2005)利用FlowCam結合葉綠素a分析化學除藻法對水體中藍藻細胞的破壞或溶解能力。通過熒光粒子濃度和葉綠素a分析,將葉綠素a的損失量化為細胞損傷。FlowCam拍攝的圖像為細胞損傷提供了定性觀察,可以更好的了解細胞損傷中裂解的風險。
生物除藻法主要通過水生生態(tài)系統(tǒng)食物鏈關系,即利用水中浮游動物和魚類對水華藻類的攝食,改變生物群落結構,增加對藻華藻量的控制能力。生物除藻法不會對環(huán)境造成二次污染,但是極易造成外來物種入侵,進而對整個生態(tài)環(huán)境系統(tǒng)造成嚴重破壞。因此,需要找到合適的臨界值,才能達到較好的控制效果。Ide等(2007)通過與傳統(tǒng)顯微鏡分析的比較,探討了使用FlowCam快速分析橈足類攝食的有效性和可靠性。結果表明,用FlowCam估計的橈足類動物的攝食率與用顯微鏡觀察浮游動物的攝食率是一致的;從顆粒的體積特異性熒光強度上,F(xiàn)lowCam成功地區(qū)分了浮游動物和浮游植物,且用時較少不到顯微計數(shù)所需時間的十分之一。因此,未來我們也可以通過FlowCam來探究鰱魚等生物進食藍藻的速率,進而估算其控制藻華所需要的數(shù)量。
物理除藻法不會造成二次污染和生物入侵,但技術成本高、操作環(huán)境差。隨著超聲波技術的發(fā)展,將超聲波用于除藻抑藻方面的研究日益增多。超聲波除藻技術以其清潔、高效、反應條件溫和等特點,在藍藻藻華控制領域有著廣闊的應用前景。2015年夏天,新澤西州的一個飲用水處理設備進行了一項研究,在超聲波浮標測試中使用了FlowCam來幫助識別物種,并通過計數(shù)細胞和測量生物體積來監(jiān)測浮標對藍藻藻華控制的效果。
結論
FlowCam實現(xiàn)了藻類細胞的快速檢測與自動分類,減少了人工操作,不但能在實驗室內進行樣品分析,還可以在野外進行實時監(jiān)測,且系統(tǒng)維護相對簡單,具有較高的實用性,*有可能實現(xiàn)有害藻類早期預警的技術方法,在實際應用中應逐步探索形成標準的監(jiān)測方法,在湖泊、海洋等生態(tài)系統(tǒng)的研究中開拓更廣闊的領域。
雖然FlowCam已經獲得廣泛應用,但是在技術上仍存在一些不足,自動分類仍然需要人工操作的輔助。FlowCam主要是根據(jù)細胞大小及色素差異對一些特定類群藻類進行識別,對于室內培養(yǎng)的純種藻分類效果較好,而野外樣品要復雜的多。一方面,赤潮藻細胞種類繁多,許多不同種類的浮游藻在形態(tài)學上極為相似;另一方面,同一種類的藻細胞在不同生長時期以及不同視點所獲取的圖像又可能在形態(tài)上具有差異性,這就使得自動識別工作非常困難;加之由于技術的限制,通常獲得的圖像分辨率較差,更在一定程度上影響了識別的準確度。當FlowCam應用于其他淺水湖泊時,需要使用者根據(jù)實際情況建立適用于該水體的藻類信息數(shù)據(jù)庫,方可實現(xiàn)部分藻類的自動分類。
參考文獻
Farrow C R, Ackerman J D, Smith R E, et al. Riverine transport and nutrient inputs affect phytoplankton communities in a coastal embayment[J]. Freshwater Biology, 2020, 65(2): 289-303.
Ide K, Takahashi K, Kuwata A, et al. A rapid analysis of copepod feeding using FlowCAM[J]. Journal of Plankton Research, 2007, 30(3): 275-281.
Jason H S, Lisa C, Tammi L R, et al. Combing new technologies for determination of phytoplankton community structure in the northern gulf of Mexico[J]. Journal of Phycology, 2005, 41(2): 305-310.
Lehman P W, Kurobe T, Lesmeister S, et al. Impacts of the 2014 severe drought on the Microcystis bloom in San Francisco Estuary[J]. Harmful Algae, 2017: 94-108.
Lomas M W, Bronk D A, Den Engh G V, et al. Use of Flow Cytometry to Measure Biogeochemical Rates and Processes in the Ocean[J]. Annual Review of Marine Science, 2011, 3(1): 537-566.
Trask B, Den Engh G J, Elgershuizen J H, et al. Analysis of phytoplankton by flow cytometry[J]. Cytometry, 2005, 2(4): 258-264.
陳雋. 肝毒性微囊藻毒素在巢湖和太湖水生動物體內的生物富集及對水產品安全性的潛在威脅[D]. 北京: 中國科學院大學, 2006.
陳小鋒, 揣小明, 楊柳燕. 中國典型湖區(qū)湖泊富營養(yǎng)化現(xiàn)狀、歷史演變趨勢及成因分析[J]. 生態(tài)與農村環(huán)境學報, 2014, 30(04): 438-443.
侯建軍, 黃邦欽, 戴相輝. 赤潮藻細胞計數(shù)方法比較研究[J]. 中國公共衛(wèi)生, 2004(08): 15-16.
胡傳林, 萬成炎, 吳生桂, 等. 藍藻水華的成因及其生態(tài)控制進展[J]. 長江流域資源與環(huán)境, 2010, 19(12): 1471-1477.
胡利靜, 肖艷翼, 蔣新益, 等. 淡水藍藻控制方法的概述[J]. 水產養(yǎng)殖, 2015, 36(02): 6-11.
孔繁翔, 高光. 大型淺水富營養(yǎng)化湖泊中藍藻水華形成機理的思考[J]. 生態(tài)學報, 2005(03): 589-595.
孔繁翔, 馬榮華, 高俊峰, 等. 太湖藍藻水華的預防、預測和預警的理論與實踐[J]. 湖泊科學, 2009, 21(03): 314-328.
李晟銘, 劉吉平, 宋開山, 等. 基于Landsat影像巢湖藍藻水華暴發(fā)時空變化特征及其驅動因素分析[J]. 長江流域資源與環(huán)境, 2019, 28(05): 1205-1213.
陸開宏. 藍藻水華與2種藻食性水生動物的相互作用[D]. 青島: 中國海洋大學, 2009.
路云霞, 吳長年, 黃戟, 等. 由“無錫太湖水華事件”論太湖富營養(yǎng)化的防治[J]. 生態(tài)經濟, 2008(02): 154-157.
孟溪. 藻類鑒定及分類方法研究進展[J]. 生物化工, 2019, 5(02): 102-104.
莫婉湫, 李策, 劉玉, 等. 認識“水華”[J]. 濕地科學與管理, 2009, 1(05): 62-63.
錢奎梅, 劉霞, 陳宇煒. 淡水浮游植物計數(shù)與定量方法[J]. 湖泊科學, 2015, 27(05): 767-775.
錢樹本, 劉東艷, 孫軍. 海藻學[M]. 青島: 中國海洋大學出版社, 2005.
王志剛. 水體浮游植物濃度原位分類測量方法研究與系統(tǒng)研制[D]. 北京: 中國科學技術大學, 2008.
肖興富, 李文奇, 劉娜, 等. 富營養(yǎng)化水體中藍藻毒素的危害及其控制[J]. 中國水利水電科學研究院學報, 2005(02): 116-123.
楊銘威, 石亞東, 孫志, 等. 太湖藍藻爆發(fā)引發(fā)無錫供水危機的思考[J]. 水利經濟, 2009, 27(03): 36-38+74-75.






